La comprensión de la relación entre los genomas humanos y los coronavirus ha avanzado significativamente, revelando cómo nuestras especies han interactuado y se han adaptado a lo largo del tiempo. Un equipo internacional de investigadores, liderado por la Universidad de Adelaida y la Universidad de Arizona, ha analizado los genomas de miles de individuos de diversas poblaciones para desentrañar las huellas genéticas de la adaptación a los coronavirus, la familia de virus responsable de brotes importantes en las últimas décadas, incluida la pandemia actual.
Los genomas humanos modernos son vastos archivos evolutivos. "Los genomas humanos modernos contienen información evolutiva que se remonta a cientos de miles de años, sin embargo, solo en las últimas décadas los genetistas han aprendido a decodificar la amplia información capturada dentro de nuestros genomas", explica Yassine Souilmi, autora principal del estudio. "Esto incluye ‘adaptaciones’ fisiológicas e inmunológicas que han permitido a los humanos sobrevivir a nuevas amenazas, incluidos los virus”.
Los virus, por su naturaleza simple, necesitan invadir células huésped para replicarse. "Los virus son criaturas muy simples con el único objetivo de hacer más copias de sí mismos. Su simple estructura biológica los hace incapaces de reproducirse por sí mismos, por lo que deben invadir las células de otros organismos y secuestrar su maquinaria molecular para existir". Esta invasión ocurre a través de la interacción con proteínas específicas de la célula huésped, conocidas como proteínas de interacción viral (VIP). El estudio identificó adaptaciones en 42 genes humanos que codifican estas VIP.
Sorprendentemente, se encontraron señales de adaptación a coronavirus en cinco poblaciones de Asia Oriental. "Encontramos señales VIP en cinco poblaciones del este de Asia y sugerimos que los antepasados de los asiáticos orientales modernos estuvieron expuestos por primera vez a los coronavirus hace más de 20.000 años", señala el Dr. Souilmi. Estas poblaciones incluyen a habitantes de China, Japón y Vietnam, regiones que, en el contexto de la pandemia actual, no experimentaron una severidad tan extrema.
Los 42 VIP identificados son particularmente activos en los pulmones, el tejido más afectado por los coronavirus. "Confirmamos que interactúan directamente con el virus subyacente a la pandemia actual". Estudios independientes han corroborado que las mutaciones en estos genes VIP pueden influir en la susceptibilidad y la gravedad de la COVID-19, y varios VIP se están investigando para el desarrollo de tratamientos. "Nuestras interacciones pasadas con virus han dejado señales genéticas reveladoras que podemos aprovechar para identificar genes que influyen en la infección y la enfermedad en las poblaciones modernas, y pueden informar los esfuerzos de reutilización de fármacos y el desarrollo de nuevos tratamientos", afirma el Dr. Ray Tobler, coautor del estudio. "Al descubrir los genes previamente afectados por brotes virales históricos, nuestro estudio apunta a la promesa de los análisis genéticos evolutivos como una nueva herramienta para combatir los brotes del futuro".
La secuenciación del genoma del SARS-CoV-2 ha sido fundamental para la investigación. El genoma completo del coronavirus de Wuhan, oficializado como SARS-CoV-2, fue publicado en el UCSC Genome Browser, una plataforma accesible para investigadores de todo el mundo. "El coronavirus de Wuhan, cuyo nombre oficial es 2019-nCoV, ya es responsable de más de 900 muertes y más de 40.000 personas infectadas en todo el mundo. Conocer el genoma del virus, así como las diferentes versiones que pueden encontrarse en los pacientes, tiene importantes aplicaciones epidemiológicas y biomédicas. Es el primer paso para investigar el origen del virus y estudiar su evolución y propagación, así como un elemento clave a la hora de desarrollar una vacuna para impedir la infección".
El genoma del SARS-CoV-2, compuesto por una sola cadena de ARN, tiene aproximadamente 30.000 letras. Su análisis permite identificar genes clave, como aquel que codifica la proteína utilizada por el virus para entrar en las células. Paralelamente, plataformas como GISAID (Global Initiative on Sharing All Influenza Data) facilitan la compartición pública de secuencias virales, acelerando la investigación global.
El SARS-CoV-2 pertenece a la subfamilia Orthocoronavirinae, dentro de la familia Coronaviridae, que se divide en cuatro géneros: Alphacoronavirus, Betacoronavirus, Gammacoronavirus y Deltacoronavirus. Estos virus son conocidos por causar diversas enfermedades en mamíferos, incluyendo infecciones respiratorias en humanos. Históricamente, otros coronavirus como el SARS-CoV (2002) y el MERS-CoV (2012) han causado brotes epidémicos graves.
La evolución del SARS-CoV-2 ha sido objeto de intenso estudio. El virus evoluciona a un ritmo aproximado de 1-2 mutaciones por mes. Se han identificado dos macro-haplogrupos principales, A y B, que se diferencian por mutaciones puntuales. Una mutación específica, la transversión A23403T, que altera la proteína Spike, ha sido asociada con una mayor transmisibilidad, lo que podría explicar la rápida propagación de ciertas cepas. La transmisión por "supercontagiadores" también juega un papel importante en la epidemiología del virus.
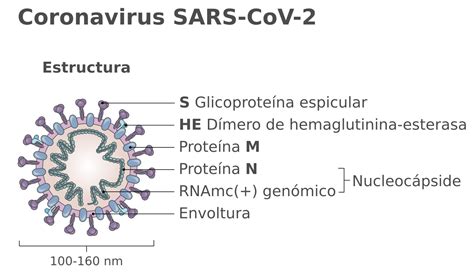
La estructura del SARS-CoV-2, con su genoma de ARN y su proteína Spike, es crucial para su ciclo de infección. La proteína Spike facilita la entrada del virus en las células humanas, y posteriormente, la maquinaria celular se utiliza para replicar el material genético viral y ensamblar nuevos virus.
El período de incubación de la COVID-19 varía, pero generalmente oscila entre 4 y 7 días, con un máximo del 95% de los casos presentando síntomas en menos de 12.5 días. Los síntomas iniciales pueden ser similares a los de la gripe, pero pueden progresar a complicaciones como neumonía y dificultad respiratoria. La respuesta inmunitaria humana implica tanto inmunidad celular como producción de anticuerpos. Si bien la presencia de anticuerpos neutralizantes puede conferir inmunidad temporal, la memoria inmunológica a través de células B de memoria parece ser más duradera.
Estudios recientes sugieren una predisposición genética a la infección por SARS-CoV-2. Variantes genéticas en el gen ACE2 en el cromosoma X podrían ofrecer protección, mientras que polimorfismos en genes como IFNAR2 y CXCR6 se han relacionado con la susceptibilidad y la gravedad de la COVID-19.
La investigación genética ha identificado 13 zonas del genoma humano asociadas con la posibilidad de contraer COVID-19 y padecer un cuadro grave de la enfermedad. Este descubrimiento, realizado por la iniciativa COVID-19 Host Genetics Initiative, involucró a miles de investigadores y pacientes a nivel mundial. Se ha observado que dos de estas zonas genómicas tienen frecuencias más altas en poblaciones de Asia Oriental y del Sur de Asia en comparación con las de ascendencia europea, resaltando la importancia de la diversidad genética en los estudios.
Entre los genes de interés se encuentra FOXP4, relacionado con el cáncer de pulmón, cuya variante genética, más frecuente en poblaciones asiáticas e hispanas/latinas, podría estar asociada a la COVID-19 severa. Otros genes implicados incluyen DPP9 (también relacionado con cáncer de pulmón y fibrosis pulmonar) y TYK2 (asociado a enfermedades autoinmunes).
¿SUSCEPTIBILIDAD GENÉTICA PARA LA ENFERMEDAD COVID-19? ESTUDIO IDENTIFICARÍA 13 GENES RELACIONADOS
La secuenciación del genoma completo del SARS-CoV-2, realizada por instituciones como la Universitat de València y FISABIO, ha sido crucial para entender la biología del virus. El genoma viral, compuesto por ARN, contiene las instrucciones para su replicación y evolución. Las mutaciones en este genoma, aunque a menudo tienen poco impacto, pueden influir en la transmisibilidad, la gravedad de la enfermedad y la eficacia de las vacunas y tratamientos.
La comparación de secuencias genómicas permite reconstruir la historia evolutiva del virus y identificar mutaciones clave. Esto es fundamental para el desarrollo de dianas terapéuticas y la comprensión de cómo el virus interactúa con las células humanas. La colaboración global en la compartición de datos genómicos, a través de plataformas como GISAID, acelera el análisis en tiempo real y fortalece las medidas de control de la epidemia.
El SARS-CoV-2, con su genoma de ARN, tiene una tasa de mutación relativamente alta, lo que permite observar cambios genéticos acumulados desde el inicio de la pandemia. El estudio de estas mutaciones es esencial para rastrear la propagación del virus y entender su evolución.
La taxonomía de los coronavirus incluye varias especies que pueden causar enfermedades en humanos, desde resfriados comunes hasta síndromes respiratorios graves. El SARS-CoV-2 se clasifica como un Betacoronavirus, similar a los virus que causaron los brotes de SARS y MERS.
El origen zoonótico del SARS-CoV-2, probablemente a partir de murciélagos, ha sido una línea de investigación importante. Se postula que un animal intermediario pudo haber facilitado el salto del virus a los humanos, similar a lo ocurrido con el SARS y el MERS. La investigación continúa para identificar este huésped intermediario.
La transmisión del virus ocurre principalmente a través de gotitas respiratorias y aerosoles, así como por contacto con superficies contaminadas. Medidas de higiene como el lavado de manos, el uso de desinfectantes y la limpieza de superficies son cruciales para prevenir la propagación. El jabón, al disolver la membrana lipídica del virus, es particularmente efectivo.
El período de incubación de la COVID-19, típicamente de unos cinco días, puede variar. Los síntomas comunes incluyen fiebre, tos seca y fatiga, pero pueden agravarse hasta incluir dificultad respiratoria. Alrededor del 15% de los casos requieren hospitalización, y un tercio de estos pueden necesitar cuidados intensivos. La tasa de mortalidad varía significativamente según la rapidez del diagnóstico y tratamiento.
Se estima que aproximadamente el 30% de los infectados son asintomáticos, pero siguen siendo contagiosos, lo que subraya la importancia del distanciamiento social y las pruebas diagnósticas.
Un síndrome similar a la enfermedad de Kawasaki ha sido reportado en niños con COVID-19, lo que ha generado preocupación y la necesidad de vigilancia médica. La enfermedad de Kawasaki es una vasculitis sistémica que puede tener complicaciones cardíacas graves.
La investigación sobre la enfermedad de Kawasaki ha revelado complejas interacciones inmunológicas, incluyendo la respuesta de citosinas y la posible implicación de factores genéticos. Estudios recientes en Italia y Reino Unido sugieren un aumento en la incidencia y severidad de la enfermedad de Kawasaki en asociación con la pandemia de COVID-19.
El genoma del SARS-CoV-2, con sus 30.000 letras, contiene las instrucciones para su replicación. La evolución viral ha llevado a la aparición de nuevas variantes, como la G614, que se ha vuelto dominante a nivel mundial. Si bien esta variante parece tener una ventaja adaptativa y se replica mejor en cultivos celulares, la evidencia sobre su mayor transmisibilidad o gravedad en humanos aún es objeto de debate científico.
La mutación en la proteína Spike es de particular interés, ya que muchas vacunas experimentales se basan en esta proteína. La posibilidad de que las mutaciones afecten la eficacia de las vacunas futuras es una preocupación importante. Sin embargo, algunos investigadores consideran que esta mutación podría estar fuera de los dominios clave para la neutralización por anticuerpos.
La vigilancia continua de la evolución viral y la compartición de datos genómicos son esenciales para comprender el impacto de las variantes y para el desarrollo de contramedidas efectivas, como vacunas y tratamientos. La Red de la OMS sobre Coronavirus (CoViNet) es un ejemplo de los esfuerzos globales para la detección temprana y el seguimiento de coronavirus y sus variantes.
La genética humana juega un papel crucial en la respuesta a la infección por coronavirus. La identificación de variantes genéticas asociadas con la susceptibilidad y la gravedad de la COVID-19 abre nuevas vías para la prevención y el tratamiento personalizado.
tags: #goku #genkidama #coronavirus