La hidrólisis es una reacción química fundamental en diversos procesos naturales e industriales. En esencia, se trata de la ruptura de enlaces químicos mediante la adición de agua. El propio nombre, derivado del griego "hydro" (agua) y "lysis" (ruptura), nos da una pista clara sobre su naturaleza: es una forma de romper una molécula determinada al hacerla reaccionar con agua.
Imagina una molécula grande, como un polímero. La hidrólisis, con la ayuda de los iones del agua, puede romper los enlaces de esa molécula, dividiéndola en fragmentos más pequeños. En términos generales, la hidrólisis es la reacción inversa a la condensación, donde dos o más moléculas se unen para formar una sola, liberando una molécula de agua como subproducto.
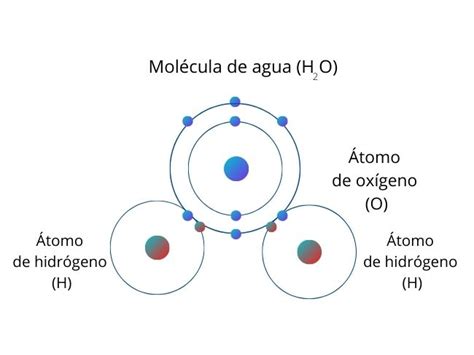
Este proceso implica la adición de una molécula de agua a un enlace, que puede ser covalente polarizado, como un enlace peptídico en una proteína o un enlace glucosídico en un carbohidrato. La molécula de agua se divide en un ion hidróxido (OH-) y un ion hidrógeno (H+), y estos se unen a los átomos del enlace que se está rompiendo.
La Hidrólisis en la Biología y la Digestión
En el ámbito de la biología, la hidrólisis es una herramienta esencial para nuestras células. Un ejemplo claro es la digestión de los alimentos. Las macromoléculas complejas que ingerimos, como proteínas, carbohidratos y grasas, se descomponen en componentes más pequeños y asimilables gracias a la hidrólisis.
Los péptidos y las proteínas, por ejemplo, están formados por aminoácidos unidos por enlaces peptídicos. Para analizar estos aminoácidos, es fundamental hidrolizar estos enlaces y liberar los aminoácidos individuales. La investigación y el desarrollo de nuevos productos químicos y biológicos a menudo utilizan la hidrólisis como una herramienta para la modificación y el estudio de moléculas grandes.
Tipos de Reacciones de Hidrólisis
Existen diversas formas en que la hidrólisis puede ocurrir:
- Hidrólisis Ácido-Base: En esta reacción, el agua se disocia en un ion hidroxilo (OH-) y un protón (H+), que se hidrata para formar un ion hidronio (H3O+). La adición de ciertas sustancias al agua puede modificar este equilibrio.
- Hidrólisis de Sales: Dependiendo de la fuerza del ácido y la base de los que provienen las sales, el pH de la disolución puede variar:
- Sal de ácido fuerte-base fuerte: No altera significativamente el equilibrio del agua, resultando en un pH neutro.
- Sal de ácido débil-base fuerte: El anión de la sal reacciona con el agua liberando iones hidroxilo, lo que produce un pH básico.
- Sal de ácido fuerte-base débil: El catión de la sal cede un protón al agua, formando iones hidronio, lo que resulta en un pH ácido.
- Sal de ácido débil-base débil: Tanto el catión como el anión reaccionan con el agua. El pH resultante dependerá de la cantidad de iones hidronio e hidroxilo producidos.
- Hidrólisis de Amidas y Ésteres: Estas reacciones pueden ocurrir en medio ácido o básico. La hidrólisis de ésteres genera ácidos carboxílicos y alcoholes, mientras que la de amidas produce aminas y ácidos carboxílicos. La saponificación, utilizada para obtener jabones a partir de triglicéridos, es un ejemplo de hidrólisis básica de ésteres.
- Hidrólisis de Polisacáridos: Los enlaces glucosídicos que unen los monosacáridos en los polisacáridos pueden romperse mediante hidrólisis, generando azúcares más simples, disacáridos o monosacáridos.
- Hidrólisis Enzimática: Algunas enzimas, conocidas como hidrolasas, catalizan específicamente estas reacciones, acelerando la descomposición de moléculas complejas.
Aplicaciones Industriales y Naturales de la Hidrólisis
La hidrólisis no se limita al ámbito biológico; sus aplicaciones son extensas:
- Producción Industrial: Se utiliza en la fabricación de ácido sulfúrico (mediante la hidrólisis del trióxido de azufre) y en la producción de celulosa a partir de madera.
- Biocombustibles: Los aceites vegetales y lípidos animales se hidrolizan para obtener ácidos grasos y glicerol, precursores de biocombustibles.
- Agricultura: La hidrólisis enzimática es clave para descomponer restos orgánicos y producir fertilizantes de alta calidad. Permite liberar nutrientes en formatos más accesibles para las plantas, optimizando la fertilización y mejorando el rendimiento de los cultivos. También se utiliza en el tratamiento y valorización de residuos agrícolas y en el desarrollo de algunos pesticidas y herbicidas.
- Mantenimiento de Piscinas: La hidrólisis juega un papel importante en la desinfección del agua de la piscina. Al descomponer moléculas contaminantes, ayuda a crear un ambiente hostil para bacterias y microorganismos. Esto puede reducir la necesidad de cloro, resultando en agua más amigable para la piel y los ojos, y una experiencia de natación más agradable al disminuir la formación de cloraminas.
Hidrólisis - en resumen
La hidrólisis ácida, a menudo realizada con HCl 6 M, es un método común para hidrolizar proteínas. Sin embargo, algunos aminoácidos pueden destruirse o no determinarse de forma fiable en estas condiciones. Para superar esto, se pueden emplear tratamientos previos como la oxidación o la alquilación para conservar ciertos aminoácidos, o recurrir a técnicas alternativas como la hidrólisis alcalina, especialmente útil para la cuantificación del triptófano.
Los procedimientos de hidrólisis pueden realizarse en fase líquida o de vapor. La hidrólisis en fase de vapor suele ser más rápida y reduce la contaminación. La elección del método de hidrólisis puede influir en la recuperación de aminoácidos específicos y en la eficacia del proceso.
La hidrólisis es, sin duda, una reacción química versátil y poderosa, indispensable para comprender y manipular procesos a nivel molecular en una gran variedad de campos.