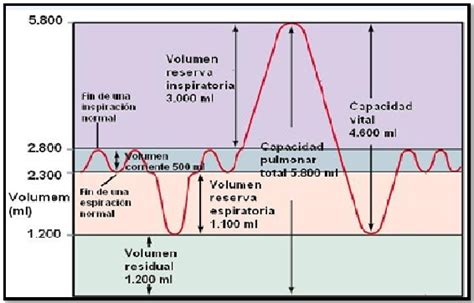
El estudio de la función pulmonar es una herramienta fundamental en la evaluación diagnóstica y el seguimiento de pacientes con enfermedades respiratorias. Además de su papel en el diagnóstico y manejo de patologías específicas, las pruebas de función respiratoria (PFR) son cruciales para la evaluación del riesgo quirúrgico, la determinación de la discapacidad y el pronóstico de diversas condiciones. La información que proporcionan estas pruebas es objetiva, precisa, reproducible y fiable, lo que las convierte en pilares del abordaje clínico.
Existen numerosas pruebas funcionales respiratorias, cada una con sus indicaciones específicas. Las PFR básicas, consideradas esenciales en la práctica clínica, incluyen la espirometría basal y la curva flujo-volumen, la prueba broncodilatadora y la gasometría arterial. Otras pruebas de gran relevancia clínica son la prueba de transferencia de monóxido de carbono (DLco), la determinación de los volúmenes pulmonares, las pruebas de provocación bronquial, las pruebas de ejercicio y la determinación de las presiones musculares máximas. En esta revisión, nos centraremos en los aspectos más relevantes de estas pruebas desde la perspectiva de la toma de decisiones clínicas, la interpretación y los puntos clave que el clínico debe considerar.
Para la realización de estas pruebas, es indispensable contar con equipos que cumplan con las normativas técnicas vigentes. La calibración de los aparatos previa a su uso, así como el seguimiento de las normas de control de infección e higiene, son igualmente imprescindibles. El personal encargado de realizar las pruebas debe poseer la experiencia y familiaridad necesarias con los equipos para garantizar la obtención de resultados de calidad. Asimismo, es fundamental que el paciente siga las instrucciones previas de preparación y comprenda cómo realizar correctamente cada prueba.
Pruebas Funcionales Respiratorias: Un Análisis Detallado
Espirometría y Curva Flujo-Volumen
La espirometría forzada, que mide el volumen espiratorio forzado en un segundo (FEV1) y la capacidad vital forzada (FVC), es la prueba de función pulmonar más accesible y útil. Su realización dura entre 10 y 15 minutos y requiere un equipo con un coste aproximado de entre 2.000 y 6.000 euros, con un coste por prueba de unos 40 euros y prácticamente sin riesgos para el paciente.
Si el espirómetro permite registrar datos durante más de 30 segundos, se puede medir también la capacidad vital lenta (SVC o VCin). La SVC aumenta la sensibilidad de la espirometría para detectar obstrucción, aunque a expensas de una mayor duración de la prueba. Otros parámetros medidos son los flujos mesoespiratorios (MEF25-75%) y los flujos máximos instantáneos al 75%, 50% o 25% de la FVC (MEF75%, 50%, 25%). Estos parámetros se consideran indicadores del estado de la vía aérea pequeña; si bien se ha observado una correlación estadística en grupos de sujetos, son muy poco sensibles debido a su variabilidad. Los puntos de corte (percentil 5%) se aproximan al 50% en sujetos mayores de 50 años.
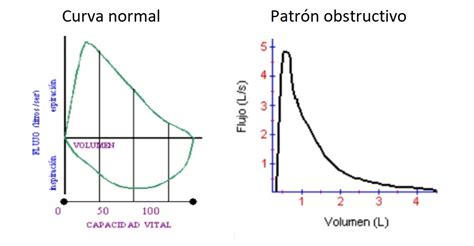
La morfología de la curva flujo-volumen es de gran utilidad para detectar la concavidad característica del enlentecimiento de la espiración a volúmenes bajos en pacientes obstructivos y la convexidad en pacientes restrictivos. Además, presenta una forma distintiva en la obstrucción de la vía aérea superior. Sin embargo, la sensibilidad es baja en estenosis traqueales de más de 1 cm de diámetro.
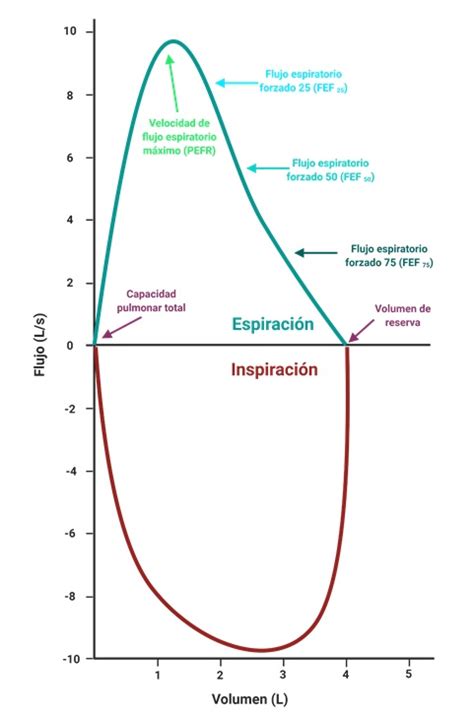
La correcta interpretación de la espirometría requiere su integración con los datos clínicos del paciente. En general, se pueden identificar patrones funcionales respiratorios: obstructivo, restrictivo y mixto. El parámetro más importante para identificar una obstrucción es una relación FEV1/VC < 70%. Sin embargo, este punto de corte puede generar un número no despreciable de falsos positivos en varones mayores de 40 años y en mujeres mayores de 50 años, así como un sobrediagnóstico de obstrucción en personas mayores, asintomáticas y no fumadoras. Por ello, se ha recomendado el uso del límite inferior del intervalo de confianza (LIN) = Valor medio predicho - (Error estándar de los residuales × 1.645)², pero su uso es limitado debido a la tradición y a que este percentil no está disponible en la mayoría de los equipos.
La espirometría también permite valorar la gravedad de la alteración ventilatoria. Para ello, se han definido categorías como marco conceptual más sencillo, en función del FEV1 post-broncodilatadores para defectos obstructivos, y según la capacidad vital (VC) o la capacidad pulmonar total (TLC) para defectos restrictivos. Los puntos de corte de las distintas normativas guardan relación con la capacidad de realizar actividades de la vida diaria, la morbilidad y la mortalidad en la EPOC. No obstante, son menos relevantes en el asma, donde la hiperreactividad, la variabilidad de la función (y de la clínica) y la respuesta al tratamiento son factores más importantes que el FEV1 puntual. Tampoco son relevantes en la obstrucción de las vías aéreas superiores.
Aunque en la mayoría de los trastornos restrictivos el empeoramiento clínico se acompaña de una pérdida de la VC, esta puede estar solo moderadamente disminuida en enfermedades pulmonares intersticiales difusas (EPID) con una marcada pérdida de la capacidad de difusión y alteraciones gasométricas graves. Se puede producir insuficiencia respiratoria grave en pacientes con enfermedades neuromusculares rápidamente progresivas que, poco antes, presentaban una VC normal o levemente disminuida.
Otro aspecto a considerar es que el FEV1 y la VC son indicadores generales de salud relacionados con la expectativa de vida, incluso en pacientes no fumadores.
La espirometría es muy útil para seguir la evolución y monitorizar los cambios funcionales a lo largo del tiempo. Se han publicado puntos de corte para considerar un cambio como significativo.
Prueba de Reversibilidad (Broncodilatadora)
La prueba de reversibilidad, con un coste adicional de unos 40 euros a la espirometría (total 80 euros), está indicada en todos los pacientes asmáticos en el momento del diagnóstico y, si persiste la obstrucción, en las espirometrías de seguimiento. Es importante advertir al paciente y al laboratorio si el objetivo es verificar la respuesta al tratamiento, para que no se retire la medicación de forma rutinaria.
La propia definición de la EPOC señala que esta enfermedad se caracteriza por «la limitación del flujo aéreo que no es reversible» y porque «no hay cambios marcados en la función en un periodo de varios meses». Esto implica que, si existe reversibilidad, esta no debe ser total, y para ello se requiere medir el FEV1/VC < 70% tras broncodilatadores. De hecho, en estudios epidemiológicos se ha observado que la prevalencia de EPOC disminuye entre el 10% y el 40% al usar el FEV1/VC post-broncodilatadores, aunque se desconoce el impacto socioeconómico de esta diferencia.
La respuesta positiva a los broncodilatadores no permite diferenciar entre EPOC y asma, aunque mejorías de más de 400 ml tras broncodilatadores o glucocorticoides sugieren la posibilidad de asma o, al menos, un fenotipo mixto.
Un concepto que ha cambiado en los últimos años es que la presencia o ausencia de broncodilatación, salvo que sea muy acusada (es decir, >400 ml), no parece predecir con suficiente exactitud el alivio sintomático, los cambios en la capacidad de ejercicio, ni la respuesta a largo plazo a corticoesteroides o broncodilatadores. Por lo tanto, la prueba de broncodilatadores no tiene valor como guía de tratamiento.
En cuanto al pronóstico, existe abundante evidencia que identifica al FEV1 como un factor de riesgo en la EPOC, y en este caso, el parámetro óptimo para el diagnóstico es el FEV1 tras broncodilatadores. Se ha encontrado que la reversibilidad se asocia a una disminución acelerada del FEV1, aunque no todos los estudios encuentran esta asociación.
El porcentaje de pacientes con EPOC que responden a broncodilatadores es variable. En el estudio UPLIFT, el 52% de los pacientes respondieron a broncodilatadores, con cifras del 64%, 48% y 18% según los estadios GOLD II, III o IV, respectivamente. Se ha observado que hasta el 35% de los pacientes con la primera prueba de broncodilatadores negativa pueden tenerla positiva en pruebas posteriores. Sin embargo, con dos pruebas se detectan la mayoría de pacientes (el 88%) que ocasionalmente pueden responder al broncodilatador, por lo que no estaría justificado su uso rutinario en pacientes con EPOC que ya tienen una o a lo sumo dos pruebas de broncodilatación anteriores.
Se puede usar cualquier fármaco broncodilatador, pero por eficiencia, casi siempre se emplea un β2-agonista inhalado de acción rápida (salbutamol a dosis de 400 μg o 4 «pufs» separados 30 s y con una correcta maniobra de inhalación), ya que su efecto comienza 5 minutos tras la inhalación y alcanza un máximo a los 20 minutos. Si se usa ipratropio, se recomienda una dosis de 160 μg (8 puffs) y realizar la espirometría «post» a los 45 minutos. Otra forma de evaluar la reversibilidad es administrar un tratamiento de prueba (ensayo terapéutico individual) y evaluar al paciente a los 30 días, advirtiendo al laboratorio y al paciente de que no se debe retirar la medicación prescrita antes de realizar la prueba de evaluación de efectividad.
Flujo Máximo Espiratorio (PEF)
El flujo máximo espiratorio (PEF) es el flujo máximo que una persona puede exhalar durante un breve esfuerzo espiratorio máximo después de una inspiración completa. En pacientes con asma, el PEF se correlaciona con el FEV1, pero no debe usarse como su sustituto. El PEF es una medición fácil de realizar con un equipo que cuesta unos 30 euros, aunque su popularidad no es muy grande.
Utilidades del PEF:
- Diagnóstico: Variaciones superiores al 20% son diagnósticas de asma en el contexto adecuado. El PEF permite observar la variabilidad en relación con ciertas exposiciones, como mejoría en vacaciones o empeoramiento al exponerse a ciertos ambientes.
- Monitorización de la enfermedad: Para ello, se debe establecer el valor inicial realizando mediciones durante 15 días en condiciones de estabilidad clínica y máximo tratamiento, y utilizar esta referencia para establecer planes de acción. Sin embargo, no es fácil mantener la adhesión a largo plazo, lo que limita su uso.
Pruebas de Provocación Inespecífica
Existen distintas pruebas de provocación inespecífica (ATP, manitol, hiperventilación isocápnica, ejercicio, colorantes alimenticios) útiles en contextos específicos. Estas pruebas requieren tiempo y su coste es de unos 200 euros.
La prueba puede estar indicada cuando el diagnóstico de asma está en cuestión (síntomas atípicos, espirometría normal), cuando un paciente es sospechoso de padecer asma ocupacional o asma inducida por irritantes, y cuando se requiere una prueba que descarte el asma en buceadores, deportistas, personal militar u otros individuos en quienes el broncoespasmo supondría un peligro inaceptable para ellos o para otras personas, o es requerido por las normas para usar medicación antiasmática y no esté contraindicada.
En los casos en que el asma se desencadene por el ejercicio, el asma de esfuerzo tenga implicaciones profesionales o ante la persistencia de síntomas con el ejercicio en un asmático correctamente tratado, pueden estar indicadas las pruebas de provocación al ejercicio o hiperventilación isocápnica.
Aunque las pruebas de provocación bronquial inespecíficas permiten valorar la gravedad del asma y monitorizar su tratamiento, no se usan habitualmente para estos fines en la clínica.
Interpretación de la prueba negativa: Descarta en general el asma, salvo en ciertos casos de asma alérgica o asma inducida por irritantes en los que la prueba se ha realizado tiempo después de la exposición y de los síntomas.
Interpretación de la prueba positiva: Aproximadamente del 1% al 7% de la población general asintomática tiene hiperreactividad bronquial (hasta el 26% si se incluyen fumadores o atópicos). Sin embargo, hay quienes piensan que estos pacientes son asmáticos leves que no perciben sus síntomas. Por lo tanto, el diagnóstico no debe basarse únicamente en una prueba de hiperreactividad positiva, y se debe confirmar que los síntomas del paciente desaparecen con el tratamiento.
Determinación de los Volúmenes Estáticos y Resistencias Pulmonares
Esta prueba determina los volúmenes y capacidades pulmonares que no se pueden medir en una espirometría, como el volumen residual (VR), la capacidad residual funcional (FRC) y la capacidad pulmonar total (TLC). Su coste es de unos 150 euros.
Los métodos más usados son el método de dilución de helio y lavado de nitrógeno (FRC), que suelen poder medirse con el mismo equipo que la difusión de monóxido de carbono, y la pletismografía corporal (FRCpleth), que requiere una cabina con un coste aproximado de 36.000 euros.