La lejía, también conocida como lavandina, es un término que engloba diversas sustancias químicas que, al disolverse en agua, actúan como potentes agentes oxidantes. Su uso principal radica en su eficacia como desinfectante, combatiendo eficazmente hongos y bacterias, además de ser un agente blanqueador y un solvente de materia orgánica. Es importante no confundirla con el elemento químico cloro (Cl) ni con la sustancia desinfectante de uso común que comparte el mismo nombre.

El elemento cloro es el componente fundamental de la mayoría de los blanqueadores modernos, como la solución de hipoclorito de sodio. Esta solución acuosa de hipoclorito de sodio solo mantiene su estabilidad en un ambiente de pH básico.
Un Largo Camino Histórico en el Blanqueo
El proceso de blanqueo tiene raíces milenarias. Las primeras técnicas documentadas consistían en exponer tejidos y telas a la acción combinada del sol y el agua en campos de blanqueo. Este método ancestral sentó las bases para el desarrollo de los blanqueadores que conocemos hoy en día.
Los avances significativos en la ciencia del blanqueo se produjeron durante el siglo XVIII. Científicos como el químico sueco Carl Wilhelm Scheele, descubridor del cloro, y los franceses Claude Louis Berthollet y Antoine Germain Labarraque, jugaron roles cruciales. Berthollet reconoció el potencial del cloro para blanquear telas y creó el primer hipoclorito de sodio, conocido como "Eau de Javel" o agua de Javel. Por su parte, Labarraque descubrió las propiedades desinfectantes de los hipocloritos.
Posteriormente, Louis Jacques Thénard produjo peróxido de hidrógeno en 1818. Aunque el peróxido de hidrógeno se utilizó por primera vez para el blanqueo en 1882, su relevancia comercial no se consolidó hasta después de 1930. A principios del siglo XX, el perborato de sodio se introdujo en el mercado, ganando popularidad en América del Norte en la década de 1980. Sin embargo, estos compuestos han sido en gran medida reemplazados por alternativas industriales como el hidróxido de sodio, el carbonato de sodio y el bicarbonato de sodio.

Composición y Mecanismos de Acción
La lejía, en su forma más común de uso doméstico, es una solución de hipoclorito de sodio. La reglamentación actual establece que las concentraciones de hipoclorito sódico en productos de uso doméstico deben oscilar entre el 3,15% y el 6,3% (equivalente a 20 y 60 g de cloro activo por litro de producto) para evitar reacciones cáusticas.
El mecanismo de acción de los oxidantes, como la lejía, se basa en su capacidad para introducir átomos de oxígeno, azufre o halógenos en otras sustancias. Al ser un álcali, cuanto mayor sea su basicidad, más severas serán las lesiones que pueda causar en el organismo. Estas lesiones pueden manifestarse como necrosis por licuefacción (donde el tejido se transforma en una masa líquida viscosa), saponificación de grasas o desnaturalización de proteínas.
Efectos de la Exposición a la Lejía
Los daños que la lejía puede ocasionar en el cuerpo humano varían considerablemente. Dependen de la vía de exposición (ingestión, contacto cutáneo o inhalación), el tiempo de exposición, las propiedades físicas del producto y la cantidad y concentración que alcanza en el organismo.
Ingestión
La ingestión de lejía afecta primariamente las mucosas de la boca, la faringe y el esófago, extendiéndose posteriormente al resto del sistema digestivo. Pequeñas cantidades pueden provocar una irritación leve de la faringe y el esófago, y raramente gastritis, ya que el pH ácido del estómago puede neutralizar cantidades mínimas.
Exposición Dental
El hipoclorito de sodio es utilizado por los dentistas en la limpieza de conductos radiculares. Su uso es seguro siempre que se mantenga confinado dentro del conducto radicular.
Inhalación
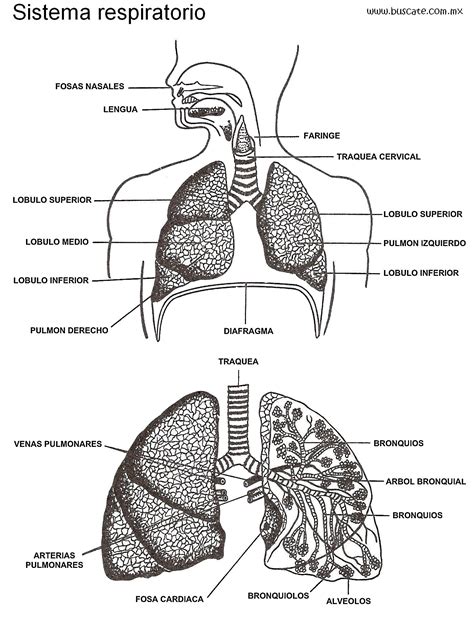
La inhalación de lejía puede afectar las mucosas del sistema respiratorio. La exposición a altas concentraciones, especialmente en espacios cerrados y sin ventilación adecuada, puede desencadenar disfonía (pérdida del timbre normal de la voz debido a lesión laríngea), dificultad respiratoria, tos, disnea (dificultad para respirar) y edema agudo de pulmón.
Exposición Cutánea
El contacto de la lejía con la piel puede resultar en irritación cutánea o hipersensibilidad dérmica. Estas reacciones pueden ser inmediatas o aparecer con cierto retraso.
Exposición Ocular
Generalmente, la exposición ocular a la lejía provoca lesiones leves. Las afectaciones más comunes son las lesiones corneales, caracterizadas por una alteración superficial del epitelio que causa molestias y ardor. La recuperación de estas lesiones suele ser rápida, ocurriendo en uno o dos días.
Toxicidad Hematológica
El hipoclorito sódico, al reaccionar con el plasma sanguíneo, puede descomponerse en agua y ácido hipocloroso. El ácido hipocloroso tiene la capacidad de inducir hemólisis al modificar las proteínas de la membrana de los glóbulos rojos.
Uso y abuso del cloro
Primeros Auxilios y Tratamiento
La identificación de una intoxicación por lejía puede facilitarse por el olor característico a cloro. En caso de exposición cutánea o ocular, se debe lavar la zona afectada inmediatamente con suero fisiológico o agua.
Si la intoxicación se debe a la ingestión de pequeñas cantidades, se recomienda diluir el producto con agua, leche o leche albuminosa. En casos de ingestión de grandes cantidades, se debe administrar leche albuminosa, protección mediante antibióticos y corticoides (estos últimos solo si se presenta edema en la faringe o glotis). La recuperación es probable si se aplica el tratamiento adecuado y de forma rápida. Es crucial destacar que el carbón activo está totalmente contraindicado en casos de intoxicación por lejía.
Estadísticas y Prevención
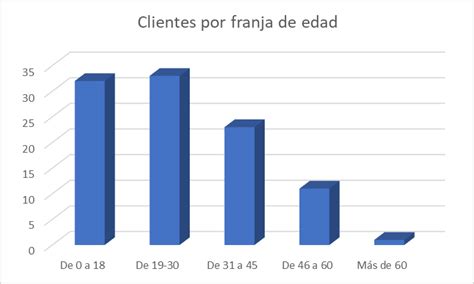
Existe información limitada sobre las tendencias estadísticas mundiales relacionadas con el envenenamiento por hipoclorito de sodio. Históricamente, las intoxicaciones por productos del hogar ocurrían de forma accidental, siendo los niños menores de 5 años los más afectados (70-80% de los casos), y en la mayoría de las ocasiones, sin requerir intervención terapéutica. Alrededor del 10% de las intoxicaciones se debían a errores de dosificación, y un 9,8% se producían de manera voluntaria en adolescentes mayores de 12 años con fines suicidas.
La prevención y la educación sobre el uso seguro de productos químicos domésticos son fundamentales para evitar accidentes y exposiciones peligrosas.